Method Article
使用患者源性肿瘤类器官的高通量 体外 检测
摘要
开发了一种高精度 的体外 高通量测定系统,以使用患者来源的肿瘤类器官(PDO)评估抗癌药物,类似于癌症组织,但不适用于具有96孔和384孔板 的体外 高通量测定系统。
摘要
患者来源的肿瘤类器官(PDO)有望成为临床前癌症模型,具有比传统细胞培养模型更好的疾病再现性。PDO已经成功地从各种人类肿瘤中产生,以准确有效地概括肿瘤组织的结构和功能。然而,在评估抗癌药物时,PDO不适合 体外 高通量测定系统(HTS)或使用96孔或384孔板进行细胞分析,因为它们的大小异质性并且在培养物中形成大簇。这些培养和测定使用细胞外基质(如基质胶)来创建肿瘤组织支架。因此,PDO具有低通量和高成本,并且很难开发出合适的分析系统。为了解决这个问题,使用PDO建立了一种更简单,更准确的HTS来评估抗癌药物和免疫疗法的效力。创建了一种 体外 HTS,它使用从在384孔板中培养的实体瘤建立的PDO。还开发了一种HTS,用于评估抗体依赖性细胞细胞毒性活性,以使用在96孔板中培养的PDO来代表免疫应答。
引言
人类癌细胞系被广泛接受用于研究癌症的生物学和评估抗癌剂。然而,这些细胞系不一定保留其源组织的原始特征,因为它们的形态,基因突变和基因表达谱可以在培养过程中长时间发生变化。此外,这些细胞系中的大多数在单层中培养或用作小鼠异种移植物,它们都不代表肿瘤组织1,2。因此,抗癌药物的临床疗效可能与在癌细胞系中观察到的疗效不同。因此,已经开发了体外系统,例如使用患者来源的肿瘤异种移植物或患者来源的肿瘤类器官(PDO)和肿瘤球体模型的离体测定,以准确再现肿瘤组织的结构和功能。越来越多的证据表明,这些模型通过与相应的癌症组织直接比较来预测患者对抗癌药物的反应。这些体外系统已经针对不同的肿瘤组织类型建立,并且还开发了用于药物筛选的相关高通量测定系统(HTS)3,4,5,6,7。近年来,从患者或患者来源的肿瘤异种移植物获得的原发性肿瘤的异质体体类器官培养物因其易于培养和维持基质组织中细胞复杂性的能力而获得了相当大的牵引力8,9,10。这些模型有望增强对癌症生物学的理解,并促进体外药物疗效的评估。
最近在福岛转化研究项目下,从不同类型的肿瘤组织(指定为F-PDO)中创建了一系列新型PDO。PDO形成大细胞簇,其形态与源肿瘤的形态相似,可以培养超过六个月11。比较组织学和全面的基因表达分析表明,即使在培养条件下长期生长后,PDO的特征也接近其源肿瘤组织的特征。此外,在96孔和384孔板中为每种类型的PDO建立了合适的HTS。这些测定用于评估几种分子靶向药物和抗体。在这里,使用来自对紫杉醇和卡铂无反应的患者的F-PDO评估用于子宫内膜癌的标准化疗药物(紫杉醇和卡铂)。因此,紫杉醇和卡铂对该PDO的细胞生长抑制活性较弱(IC50:>10μM)。此外,先前的研究表明,一些F-PDO对化疗剂和分子靶向剂的敏感性与临床疗效一致11,12,13。最后,使用三维细胞分析系统12,13分析了抗癌剂引起的PDO高阶结构的变化。使用基于PDO的HTS评估抗癌药物的结果与这些药物获得的临床结果相当。在这里,提出了一种更简单,更准确的HTS方案,可用于评估使用PDO模型的抗癌剂和免疫疗法的效力。
研究方案
所有涉及人源材料的实验均根据《赫尔辛基宣言》进行,并事先获得福岛医科大学伦理委员会的批准(批准号分别为1953年和2192年;批准日期分别为2020年3月18日和2016年5月26日)。从提供本研究中使用的临床标本的所有患者那里获得了书面知情同意。
1. PDO的培养
注意:F-PDO形成细胞簇,表现出各种异质形态并在悬浮培养物中生长(图1)。此外,F-PDO可以培养超过6个月,并且可以冷冻保存以备将来使用。
- 储存的 PDO 解冻(第 0 天)
- 在第0天解冻和种子PDO(例如,RLUN007,肺腺癌)(图1)。首先,将15mL含有1%B-27补充剂和30ng / mL表皮生长因子的PDO培养基(见 材料表)加入无菌的50mL离心管中。
- 从液氮储存中取出冷冻小瓶后,在37°C水浴中轻轻搅拌PDO2分钟。接下来,从水浴中取出小瓶,用70%乙醇擦拭小瓶,然后将小瓶移入生物安全柜中。
- 将小瓶的内容物转移到含有15mL用于PDO的培养基的管中。用3 mL移液器轻轻上下移液五次,混合PDO和培养基。在〜25°C下以200×g离心管3分钟,并弃去上清液。 将PDO沉淀重悬于5mL新鲜培养基中,并转移到25 cm2烧瓶中,轻轻移液。 最后,在37°C的培养箱中培养PDO,浓度为5%CO2。
- 每周更换两次培养基(第3-7天)。离心PDO悬浮液以沉淀细胞簇,并更换4mL培养基(80%体积)。将细胞重悬于新鲜培养基中。
注意:大多数RLUN007显示为直径为100-500μm的细胞簇。当介质中酚红的颜色变为黄色时, 如图1A所示,更频繁地更换介质。如果培养基在置换后的第二天变黄,并且每个细胞簇合并形成直径>500μm的较大簇,则以1:2的分裂比通过。 - PDO的传代培养(第8-28天)
注意:鉴于实际测量单个细胞数量的困难,传代时间是根据适当的细胞簇密度和离心后PDO沉淀的大小确定的(图1B)。在RLUN007的情况下,PDO沉淀的体积在解冻后约2周达到30μL(25 cm2 烧瓶中的饱和密度)。- 为了从一个25 cm2烧瓶转移到两个25 cm2烧瓶(P1),将PDO悬浮液转移到离心管中,并在约25°C下以200×g离心2分钟。 估计PDO沉淀的体积,并丢弃上清液。使用5 mL移液器将PDO沉淀重悬于5mL新鲜培养基中。用移液器在低速下轻轻地上下移液五次。然后,将PDO悬浮液(2.5 mL)的一半体积转移到两个烧瓶中,并向每个烧瓶中加入2.5mL新鲜培养基。将细胞在37°C下培养在5%CO2中。
- 对于从两个25 cm2烧瓶转移到一个75 cm2烧瓶(P2),将PDO悬浮液从两个烧瓶转移到两个离心管中,并在约25°C下以200×g离心PDO2分钟。 接下来,估计PDO沉淀的体积,并将沉淀重悬于2.5mL新鲜培养基(每管)中。此后,将一个管中的PDO悬浮液与另一个管中的PDO悬浮液混合,并将其转移到含有10mL新鲜培养基的75 cm2烧瓶中。将细胞在37°C下培养在5%CO2中。在第一次传代后约1周将亚培养的PDO从两个25 cm 2烧瓶转移到一个75 cm2烧瓶中(图1C)。
2. 生长抑制HTS
注意:通过测量细胞内ATP含量来评估抗癌剂对PDO的生长抑制活性,如图 2所示。该步骤使用市售的细胞活力测定试剂盒(见 材料表)进行。
- 在第0天,在烧瓶中培养PDO(例如RLUN007),直到有足够数量的细胞簇可用于测定。在播种前一天,将PDO悬浮液从75 cm2烧瓶转移到15 mL管中,并以200×g离心2分钟以测量PDO沉淀体积。然后,将PDO沉淀重悬于15mL新鲜培养基中,并将其转移回75cm2烧瓶中。将细胞在37°C下培养在5%CO2中。
注意:所需的PDO沉淀体积取决于每个PDO的稀释速率和用于测定的384孔板的数量。对于RLUN007,需要200μL细胞沉淀体积才能接种到10个384孔板中。 - 在第1天(更换培养基后24小时),使用含有70μm目过滤器的过滤器支架使用细胞碎裂和分散设备(见材料表)切碎PDO。然后,将15mL的PDO悬浮液稀释10倍。使用细胞悬浮液分配器将40μLPDO悬浮液接种到384孔超低连接球体(圆底)微孔板(见材料表)中。
注意:对于切碎细胞簇,建议使用市售的细胞片段化和分散设备(见 材料表)。 - 在接种后24小时(第2天),使用液体处理器用0.04μL测试剂溶液处理PDO,最终浓度范围为20μM至1.0nM(10个连续稀释液)(见 材料表)。
- 在第8天(测试物质处理后144小时),将细胞内ATP测量试剂加入测试孔中。使用混合器混合板并在25°C下孵育10分钟。 使用读板器测量作为发光的细胞内ATP含量(见 材料表)。
- 为了计算细胞活力,将测试孔中的ATP量除以包含载体的对照孔中的ATP量,并减去背景。为了计算6天内的生长速率,将车辆控制井中的ATP数量除以播种后24小时车辆控制井中的ATP量。
- 使用生物数据分析软件从剂量 - 反应曲线中计算50%的抑制浓度(IC50)和曲线下面积(AUC)值(见 材料表)。Z 因子是一个无量纲参数,范围从 1(无限分离)到 <0,定义为 Z = 1 - (3σc+ + 3σc-) / |μc+ - μc-|,其中 σc+、σc-、μc+ 和 μc- 分别是高 (c+) 和低 (c−) 控制14的标准差 (σ) 和平均值 (μ)。
3. HTS具有细胞拾取和成像系统,用于抑制生长
注意:如果使用方案2的数据中存在较大的偏差(当测定时的变异系数[CV]大于20%),则可以使用细胞拾取和成像系统将选定大小的PDO接种到96孔或384孔板中(图2)。该协议与上一节中的步骤 2.1 和 2.2 中描述的协议相同。该步骤是使用市售的细胞拾取和成像系统执行的(请参见 材料表)。
- 在第1天,在细胞拾取和成像系统上设置一个384孔超低附着球体微孔板,其中40μL培养基/孔作为目标板。
- 用6 mL培养基填充拣选室(见材料表),并以1,500×g离心2分钟以除去气泡。将悬浮在培养基中的PDO(PDO沉淀体积,4μL)加入拣选室并设置在系统上。
- 将腔室静置至少1分钟,然后分散,使细胞簇沉降在腔室底部;然后,对腔室进行扫描。
- 在系统上将拾取尺寸设置为140-160μm(面积15,386-20,000μm2),以自动选择细胞簇。接下来,检查扫描图像上所选细胞簇的质量,并使用拾取技巧(参见材料表)将每个孔中的十个细胞簇转移到目标板中。
- 从步骤 2.3 开始执行协议步骤。
4. HTS治疗抗体依赖性细胞毒性
注:此步骤是使用市售系统(见 材料表)执行的,该系统是一种电阻抗测量仪器。它用于通过单克隆抗体和自然杀伤(NK)细胞的抗体依赖性细胞毒性(ADCC)评估PDO的细胞溶解(图3)。NK细胞是按照制造商的说明,使用NK细胞生产试剂盒(见 材料表)从外周血单核细胞中生产的。
- ADCC活性的测量
- 在第0天,在4°C下用50μL10μg/ mL纤连蛋白溶液(0.5μg/孔)涂覆96孔板( 见材料表)过夜。
- 在第1天,在除去纤连蛋白溶液后,向每个孔中加入50μL培养基以测量背景阻抗。
- 在接种之前,将5mL细胞培养解离试剂(见 材料表)加入PDO(RLUN007:100μLPDO沉淀在75cm2 烧瓶中),并在37°C的CO2 培养箱中孵育20分钟以分散PDO。要停止胰蛋白酶消化,加入5mL培养基,离心并除去解离试剂。用新鲜培养基冲洗PDO,并通过40μm细胞过滤器过滤(见 材料表)。
- 使用细胞活力分析仪计算细胞数量(见 材料表)。
- 将PDO悬浮液转移到储液槽并使用多通道移液器混合。将PDO悬浮液加入96孔板中以5×104 个细胞/孔的孔中。每个孔包含100μL的最终体积。然后,将板置于约25°C的生物安全柜中30分钟。
- 将板转移到37°C的CO2 培养箱中的仪器中。 每15分钟记录阻抗信号的变化作为细胞指数。
- 在PDO接种的同一天在37°C水浴中解冻NK细胞。将细胞从小瓶转移到含有10 mL培养基的15 mL管中(见材料表),并在约25°C下以300×g离心5分钟。 弃去上清液并将细胞沉淀重悬于10mL新鲜培养基中。细胞计数后,将细胞密度调节至1×106个细胞/ mL并转移到75cm2烧瓶中。在37°C的5%CO2培养箱中培养NK细胞。
- 第2天,在无菌V-bottom 96孔板中以终浓度的10倍制备抗体溶液(磷酸盐缓冲盐水)。
- 从每个孔中取出60μL培养基,并向PDO中加入10μL曲妥珠单抗或西妥昔单抗溶液(10μg/ mL,1μg/ mL和0.1μg/ mL)。将板移回培养箱中的仪器并记录细胞指数1小时。
- 将NK细胞悬浮液转移到50mL管中并计数细胞数。将细胞以300×g离心5分钟,并将NK细胞密度调节为1×106个细胞/ mL和2 x 106个细胞/ mL,用于PDO的培养基。
- 以1:1或2:1的目标(RLUN007)细胞比例向效应子(NK)细胞中加入50μLNK细胞悬浮液。抗体的最终浓度为1 μg/mL、0.1 μg/mL和0.01 μg/mL。将板保持在约25°C下15分钟,然后将板返回仪器。
- 数据收集和分析
- 使用分析软件将细胞指数转换为细胞溶解百分比值(见 材料表)。
- 细胞溶解百分比是指NK细胞与单独作为对照的靶细胞(PDO)杀死的靶细胞的百分比。在每个时间点从样品孔的索引中减去仅包含NK细胞的孔的细胞指数。在添加抗体之前,立即将每个值归一化为细胞指数。使用以下等式将归一化细胞指数转换为细胞溶解百分比:细胞溶解百分比=(1 - 归一化细胞指数[样品孔])/归一化细胞指数(仅靶孔)x 100。
结果
使用PDO和384孔微孔板开发出高精度HTS来评估抗癌剂,并且以前报道过为每个PDO开发HTS10,11,12,13。通过计算简历和Z'因子来评估HTS的性能。Z'因子是一种被广泛接受的验证测定质量和性能的方法,如果该值为>0.514,则该测定适用于HTS。使用RLUN007的384孔板测定中的对照基准点显示出很小的变异性,CV值为5.8%,计算的Z'因子为0.83,如图4所示。这些结果表明,该测定对HTS具有高性能。为了研究PDO对使用HTS抗癌药物的敏感性,使用8种抗癌药物治疗的RLUN007评估生长抑制,特别是表皮生长因子受体(EGFR)抑制剂(阿法替尼,厄洛替尼,吉非替尼,拉帕替尼,奥西替尼和罗西替尼)和紫杉醇,这是非小细胞肺癌的标准临床治疗,丝裂霉素C作为阳性对照。每个PDO的抗癌剂的IC50和AUC值如图4所示。RLUN007对所有EGFR抑制剂和其他抗癌剂均表现出高灵敏度(IC50 < 2 μM,AUC < 282)。针对所有数据计算的Sigmoid曲线表明,抗癌剂的生长抑制活性可以准确测量。
当使用上述方法的数据差异很大时,将使用细胞拾取和成像系统。细胞拾取和成像系统可准确挑选细胞簇而不会损坏它们,通过对齐细胞簇大小以从测定系统中排除细胞碎片,从而实现准确的HTS测定。不使用系统时,CV值为26.0%,Z'因子值为0.23(数据未显示)。然而,使用该系统,CV和Z'因子值分别提高了6.4%和0.81。
为了使用电阻抗测量仪(长时间监测细胞的数量,形态和附着)来研究具有ADCC活性的PDO的细胞溶解,使用用抗体(曲妥珠单抗和西妥昔单抗)和NK细胞作为效应细胞在96孔板中处理的RLUN007评估阻抗信号的变化。与仅由靶细胞组成的对照相比,细胞溶解百分比随时间增加。6小时后,在没有抗体的情况下,以1:1(图5A,C)或2:1(图5B,D)的E:T比达到45%或75%。使用曲妥珠单抗的NK细胞介导的细胞溶解分别为1:1(图5A,1μg/mL)和2:1(图5B,1μg/mL)的比例约为60%和90%。相反,西妥昔单抗对NK细胞介导的细胞溶解具有剂量依赖性影响(图5C,D)。在西妥昔单抗的最高浓度下,RLUN007分别以1:1和2:1的比例以90%和100%被破坏(图5C,D)。曲妥珠单抗的效果弱于西妥昔单抗,只有60%的细胞毒性。这些结果表明,PDO测定系统可以使用基于阻抗的实时技术评估ADCC活性。
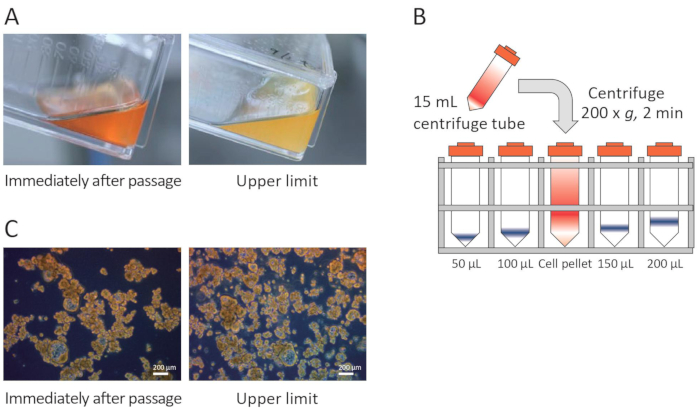
图1:PDO培养的要点。(A) 介质中的颜色变化。(B) 通过衬里含有PDO的离心管来测量PDO的量,其管标有50-200μL(C)PDO密度。请点击此处查看此图的放大版本。
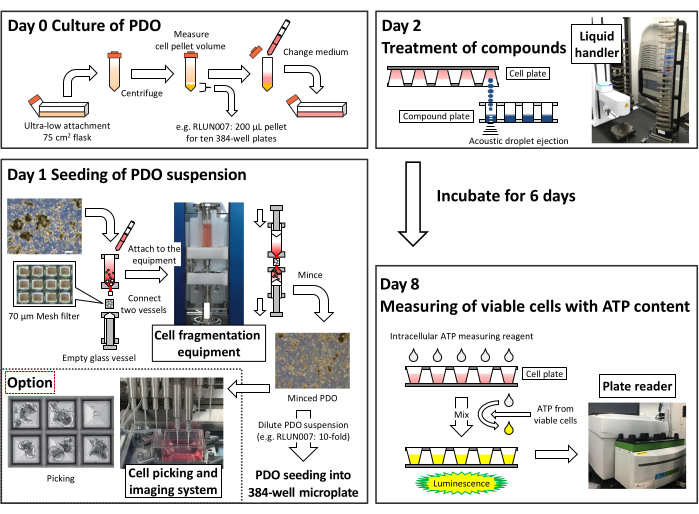
图2:用于使用384孔微孔板创建高通量测定系统的方案摘要。 请点击此处查看此图的放大版本。

图3:ADCC活性高通量测定方案摘要。 ADCC,抗体依赖性细胞毒性;NK,自然杀手。 请点击此处查看此图的放大版本。
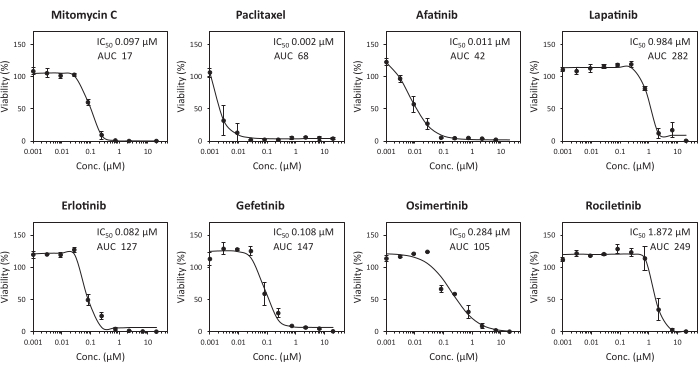
图4:用于抗癌剂抑制生长的高通量测定系统。 RLUN007抗癌药物的剂量反应曲线。将切碎的PDO接种在384孔板中。用10种不同浓度的抗癌剂(10μM至1.5nM)处理6天。数据表示一式三份实验的均值±标准差。 请点击此处查看此图的放大版本。
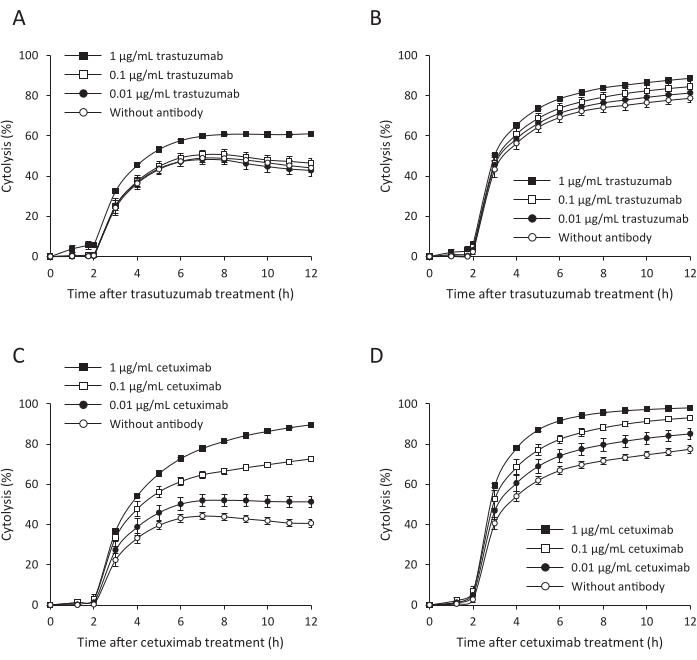
图5:ADCC活性的高通量测定。 (A,B)曲妥珠单抗。(C,D)西妥昔单抗。(A,C)RLUN007与效应细胞的1:1比例。(B,D)RLUN007比率的细胞溶解:效应细胞为1:2。在加入效应细胞后12小时测量活性。数据显示为三个重复样本的均值±标准差。ADCC,抗体依赖性细胞毒性。 请点击此处查看此图的放大版本。
讨论
PDO的独特之处在于,它们在培养或测定过程中不会酶促分离成单细胞,并且在培养物中保持细胞簇。因此,在显微镜下无法准确计数细胞的数量。为了解决这个问题,通过衬里含有细胞的离心管来直观地确定细胞的数量,其管标有50-200μL的水平(图1B)。此外,由于难以直观地测量在25 cm2烧瓶中培养的细胞簇的沉淀体积,因此使用培养基的颜色从红色变为黄色以及单个细胞或碎片的显着增加来确定传代时间作为指标(图1A,C)。这是 PDO 的传递点。在每次更换培养基时,在离心后目视测量PDO颗粒的数量。当沉淀体积停止增加,并且培养基在培养基更换后的第二天变黄时,介质被认为密度饱和,并进行传代。为每个PDO定义颗粒体积。如果PDO不增殖,则培养基交换时培养基的数量从80%变为50%,并且PDO在培养物中的密度增加。
开发了适用于PDO的HTS。其通量是使用一个75 cm 2 PDO烧瓶进行的至少10至20 个384孔板,并且每天处理的板数至少为50个。此外,HTS使用PDO对各种抗癌药物的评估结果已经报道。
在执行HTS时,通过使用单元碎片和分散设备切碎F-PDO引起的网格过滤器堵塞,首先通过将过滤器的网格尺寸更改为100μm来解决。下一步是减少施加在玻璃容器上的PDO悬浮液的体积。在制备HTS的测试物质溶液时,低分子量化合物通常溶解在二甲基亚砜中,抗体溶解在磷酸盐缓冲盐水中。使用适当的溶剂作为测试物质,并从所使用的溶剂中获得控制数据。
以下是如何处理测定数据中变异性的描述。如果使用384孔板的测试中数据存在较大差异,则应将测定板更改为96孔板格式。接种板后,还检查PDO稀释因子(接种细胞簇的数量)。最后,细胞拾取和成像系统可用于选择用于测定的PDO的大小。在将PDO添加到腔室之前,应通过低速离心除去单个细胞和小细胞簇,以便能够正确识别PDO。如果在将PDO添加到腔室后可以看到单个细胞或小细胞簇,则可以进行多次分散以除去单个细胞。接下来,尽管细胞拾取和成像系统具有允许板保持温暖的功能,但由于系统长时间工作时培养基的蒸发,因此不使用此功能。最后,细胞簇的体积是未知的,因为它可以通过平面图像识别。此外,如果两个或多个 PDO 重叠,则无法正确识别单个 PDO。但是,可以使用 remove 功能删除不需要的 PDO,方法是在移动后在扫描的图像上检查它们。
电阻抗测量仪通常用于贴壁靶癌细胞,以监测细胞增殖过程中阻抗的变化。因此,未检测到非粘附PDO的细胞指数变化。为了解决这个问题,有必要根据PDO的类型研究PDO密度和酶处理(细胞解离酶和处理时间)等播种条件。板中的孔还必须涂有适当的细胞外基质,以便接种PDO。PDO在没有酶处理的情况下接种,具体取决于PDO的类型。RLUN007用于测量阻抗,方法是在通过酶处理分散后,将PDO接种在96孔板上。将RLUN007用细胞培养物解离试剂在37°C下处理20分钟以分散细胞并将其附着在96孔板的孔中。鉴于解离的RLUN007细胞立即形成聚集体,因此希望在使用过滤器过滤后立即在板上接种。将细胞悬浮液从管转移到储液槽后,将储液器从右向左轻轻移动两到三次,并在接种到平板上之前上下移液五次。悬架也与井的每次添加混合。然后将板置于生物安全柜中30分钟(对于PDO)或15分钟(对于NK细胞),以使细胞均匀分布在孔中。第二个要点是,用抗体和NK细胞治疗的时间应该在细胞指数达到平台并且值不小于0.5之前发生。在RLUN007的情况下,开始测定的最佳时间是接种后20-22小时,接种的细胞数为5×104 个细胞/孔。
一般来说,肿瘤类器官的培养和测定使用细胞外基质如基质来产生肿瘤组织支架或酶如胰蛋白酶和胶原酶来破坏类器官3,4,5,6,7。该方法的优点是,在培养和测定过程中不需要细胞外基质或酶处理(使用电阻抗测量仪器的测定除外),这大大降低了劳动力需求和成本。此外,该方法相对容易适应HTS测定系统和各种测量系统。然而,对于某些研究目的,使用细胞外基质是可取的,因为它可以充当细胞的支架并影响组织中的形态发生,分化和稳态。
在这项研究中,使用对EGFR抑制剂临床敏感且EGFR基因高表达(数据未显示)的EGFR突变(L858R)的PDO(RLUN007)来评估EGFR抑制剂。证明RLUN007对EGFR抑制剂的敏感性高于其他肺癌衍生的F-PDO13(图4)。因此,使用PDO的HTS保留了肿瘤组织的特征,对于评估潜在的抗癌药物具有优越性,并为药物评估和个性化医学的进步提供了机会。虽然HTS适用于药物的初始筛选,但它不会再现肿瘤微环境,因此不能评估药物在体内的疗效。因此,在没有动物模型的情况下,一种可以通过与血管内皮细胞和其他基质细胞或器官芯片技术共培养来模拟人体体内肿瘤组织的体外系统正在开发中。
披露声明
Fujifilm Wako Bio Solutions Corporation是Fujifilm Wako Pure Chemicals的子公司,Fujifilm Wako Pure Chemicals是F-PDO和F-PDO媒体的商业所有者。
致谢
我们要感谢提供本研究中使用的临床标本的患者。这项研究得到了福岛县转化研究计划的资助。
材料
| Name | Company | Catalog Number | Comments |
| 384-well Ultra-Low Attachment Spheroid Microplate | Corning | 4516 | Plates for HTS |
| 40-µm Cell Strainer | Corning | 352340 | |
| AdoptCell-NK kit | Kohjin Bio | 16030400 | Kit for NK cell production |
| Cancer Cell Expansion Media plus | Fujifilm Wako Pure Chemical | 032-25745 | Medium for F-PDO |
| ALyS505N-175 | Cell Science & Technology institute | 10217P10 | Medium for NK cells |
| CELL HANDLER | Yamaha Motor | - | Cell picking and imaging system |
| CellPet FT | JTEC | - | Cell fragmentation and dispersion equipment |
| CellTiter-Glo 3D Cell Viability Assay | Promega | G9683 | Cell viability luminescent assay, intracellular ATP measuring reagent |
| Echo 555 | Labcyte | - | Liquid handler |
| EnSpire | PerkinElmer | - | Plate reader |
| E-plate VIEW 96 | Agilent | 300601020 | Plates are specifically designed to perform cell-based assays with the xCELLigence RTCA System |
| Fibronectin Solution | Fujifilm Wako Pure Chemical | 063-05591 | Plate coating for xCELLigence RTCA System |
| F-PDO | Fujifilm Wako Pure Chemical or Summit Pharmaceuticals International | - | The F-PDO can be purchased from Fujifilm Wako Pure Chemicals or Summit Pharmaceuticals International |
| Morphit software, version 6.0 | The Edge Software Consultancy | Biological data analysis software | |
| Multidrop Combi | ThermoFisher Scientific | 5840300 | Cell suspension dispenser |
| Precision Chamber | Yamaha Motor | JLE9M65W230 | Chamber for picking cell clusters using CELL HANDLER |
| Precision Tip | Yamaha Motor | JLE9M65W300 | Micro tip for picking cell clusters using CELL HANDLER |
| RLUN007 | Fujifilm Wako Pure Chemical or Summit Pharmaceuticals International | Lung tumor derived F-PDO | |
| TrypLE Express | ThermoFisher Scientific | 12604021 | Cell culture dissociation reagent |
| Ultra-Low Attachment 25 cm² Flask | Corning | 4616 | Culture flask for PDO |
| Ultra-Low Attachment 75 cm² Flask | Corning | 3814 | Culture flask for PDO |
| Vi-CELL XR Cell Viability Analyzer System | Beckman coulter | - | Cell viability analyzer |
| xCELLigence immunotherapy software, version 2.3 | ACEA Bioscience | - | Analysis software for xCELLigence RTCA System |
| xCELLigence RTCA System | ACEA Bioscience | - | Electrical impedance measuring instrument for cytolysis |
参考文献
- Sharma, S. V., Haber, D. A., Settleman, J. Cell line-based platforms to evaluate the therapeutic efficacy of candidate anticancer agents. Nature Reviews Cancer. 10 (4), 241-253 (2010).
- Shamir, E. R., Ewald, A. J. Three-dimensional organotypic culture: experimental models of mammalian biology and disease. Nature Reviews Molecular Cell Biology. 15 (10), 647-664 (2014).
- Xu, H., et al. Organoid technology and applications in cancer research. Journal of Hematology & Oncology. 11 (1), 116 (2018).
- Palechor-Ceron, N., et al. Conditional reprogramming for patient-derived cancer models and next-generation living biobanks. Cells. 8 (11), 1327 (2019).
- Broutier, L., et al. Human primary liver cancer-derived organoid cultures for disease modeling and drug screening. Nature Medicine. 23 (12), 1424-1435 (2017).
- Du, Y., et al. Development of a miniaturized 3D organoid culture platform for ultra-high-throughput screening. Nature Reviews Molecular Cell Biology. 12 (8), 630-643 (2020).
- van de Wetering, M., et al. Prospective derivation of a living organoid biobank of colorectal cancer patients. Cell. 161 (4), 933-945 (2015).
- Meijer, T. G., Naipal, K. A., Jager, A., van Gent, D. C. Ex vivo tumor culture systems for functional drug testing and therapy response prediction. Future Science OA. 3 (2), (2017).
- Inoue, A., et al. Current and future horizons of patient-derived xenograft models in colorectal cancer translational research. Cancers (Basel). 11 (9), 1321 (2019).
- Hum, N. R., et al. Comparative molecular analysis of cancer behavior cultured in vitro, in vivo, and ex vivo. Cancers (Basel). 12 (3), 690 (2020).
- Tamura, H., et al. Evaluation of anticancer agents using patient-derived tumor organoids characteristically similar to source tissues. Oncology Reports. 40 (2), 635-646 (2018).
- Takahashi, N., et al. An in vitro system for evaluating molecular targeted drugs using lung patient-derived tumor organoids. Cells. 8 (5), 481 (2019).
- Takahashi, N., et al. Construction of in vitro patient-derived tumor models to evaluate anticancer agents and cancer immunotherapy. Oncology Letters. 21 (5), 406 (2021).
- Zhang, J. H., Chung, T. D., Oldenburg, K. R. A simple statistical parameter for use in evaluation and validation of high throughput screening assays. Journal of Biomolecular Screening. 4 (2), 67-73 (1999).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。