Method Article
عزل الحمض النووي الريبي من الجنينية التجميعي واسماك الزرد [كدنا] لتحليل الجينات
In This Article
Summary
العزلة ذات جودة عالية ، RNA سليمة هو خطوة أساسية في بروتوكولات مختبر كثيرة. هنا ، علينا أن نظهر استخراج الحمض النووي الريبي من الأجنة الزرد كله والتوليف [كدنا] لاحقة في تطبيق إجراءات التجريبية المختلفة بما في ذلك التعبير الجيني التحليل ميكروأري.
Abstract
العديد من الإجراءات المختبرية هامة ومعقدة تتطلب مدخلات عالية من الحمض النووي الريبي ، ونوعية سليمة. ويمكن لعينة المتدهورة أو وجود شوائب تؤدي إلى نتائج كارثية في مجال التطبيقات التجريبية المصب. ومن ثم فهي ذات أهمية قصوى لاستخدام تقنيات متينة مع العديد من الضمانات والضوابط لمراقبة الجودة لضمان عينة متفوقة. هنا ، نحن من التفصيل على بروتوكول لعزل الحمض النووي الريبي من مجموع الأجنة الزرد بأكملها باستخدام ممسخ الكيميائية المتاحة تجاريا وتنظيف لاحقة لإزالة آثار الحمض النووي والشوائب باستخدام الحمض النووي الريبي عزلة تجارية عدة. كما RNA غير مستقر نسبيا ، وعرضة للانقسام بسهولة بواسطة RNAses ، ومعظم البروتوكولات التعبير الجيني فحص باستخدام المنتج الذي يتم تصنيعه [كدنا] مباشرة من قالب الحمض النووي الريبي. نحن من التفصيل إجراء لتحويل الحمض النووي الريبي في الناتج [كدنا] أكثر استقرارا استخدام عدة متاحة تجاريا. طوال هذه الإجراءات هناك العديد من الضوابط لمراقبة الجودة لضمان أن العينة ليست متدهورة أو ملوثة. المنتج النهائي من هذه البروتوكولات هو [كدنا] التي هي مناسبة لتحليل ميكروأري ، RT PCR أو تخزين طويل الأجل.
Protocol
الجزء 1 : استخراج الحمض النووي الريبي مجموع باستخدام الكاشف TRIzol
عند العمل مع الجيش الملكي النيبالي من المهم جدا للعمل في بيئة خالية من RNAses. احتياطات بسيطة مثل وجود ماصات محفوظة للاستخدام فقط مع الإجراءات RNA والرش في منطقة عمل مع كاشف المطهر (على سبيل المثال ، ريبونوكلياز ذهاب) قبل بداية الإجراء هي مفيدة جدا.
- للوصول الى كمية كافية من الحمض النووي الريبي تجمع الأجنة الزرد 50 مل في أنبوب microfuge 1.5 وإزالة المياه وأكبر قدر ممكن مع ماصة.
- إضافة على الفور 250 ميكرولتر من كاشف TRIzol 1 إلى الأنبوب microfuge تحتوي على الأجنة. TRIzol كاشف يحتوي على الفينول ، وينبغي أن تستخدم إلا تحت غطاء الدخان.
- ليز والتجانس الأجنة مع مدقة بيليه (حوالي 20 السكتات الدماغية) حتى يتم تعطيل بما فيه الكفاية الأنسجة.
- عندما تكون متجانسة بما فيه الكفاية الخلايا ، إضافة كاشف 750 TRIzol ميكرولتر لتساوي مجموع حجم 1 مل.
- السماح التفكك الكامل للمجمعات البروتين النووي ، احتضان عينات متجانسة لمدة 5 دقائق في درجة حرارة الغرفة. في هذه المرحلة ، يمكن أن تكون العينة فلاش مجمدة في النيتروجين السائل وتخزينه في -80 لا يمكن أن تستمر درجة مئوية أو البروتوكول.
- إضافة إلى مواصلة 0.2 مل من الكلوروفورم والصخور الأنبوب لمدة 15 ثانية لالمزيج.
- احتضان العينة لمدة 2 دقيقة في درجة حرارة الغرفة ثم الطرد المركزي في 12000 XG لمدة 15 دقيقة على 4 درجات مئوية.
- سوف الخليط منفصلة في مرحلة الفينول كلوروفورم أقل الحمراء ، الطور البيني إليه ، وعديم اللون المائي المرحلة العليا. المرحلة العليا مائي يحتوي على الحمض النووي الريبي. يجب على الطبقة العليا تتألف من حوالي 60 ٪ من الحجم الأصلي للTRIzol (حوالي 0،6 مل). نقل الطبقة العليا مائي في أنبوب microfuge جديدة باستخدام ماصة 1 مل والحرص على عدم نقل أي من طبقة الطور البيني.
- لترسيب الحمض النووي الريبي إضافة 0.5 مل الأيزوبروبانول.
- السماح للعينة على الجلوس في درجة حرارة الغرفة لمدة 10 دقائق ، وأجهزة الطرد المركزي ثم في العينة 12000 x ج لمدة 10 دقائق في 4 درجات مئوية. والحمض النووي الريبي تشكيل بيليه يشبه الهلام على الجزء السفلي من الأنبوب.
- من دون إزعاج بيليه ، إزالة طاف مع ماصة ، ويغسل بيليه في 1 مل من الإيثانول بنسبة 75 ٪. خلط عينة من قلب لطيف والطرد المركزي في XG 7500 لمدة 5 دقائق في 4 درجات مئوية.
- بعد الطرد المركزي ، وإزالة الايثانول مع ماصة ، والسماح ليجف في حين أن نموذج مقلوب لمدة 10 دقيقة.
- Resuspend وبيليه وذلك بإضافة 100 ميكرولتر من ريبونوكلياز خالية من المياه ، واحتضان العينة في 55 دقيقة لمدة 10 درجة مئوية. فمن المستحسن لدوامة الاصبع بشكل متكرر خلال حضانة للمساعدة في معالجة الجفاف الحمض النووي الريبي. اختياريا ، يمكنك التأكد من جودتها وكمية العينة باستخدام ND - 1000 NanoDrop معمل أو تواصل مباشرة إلى الخطوة التالية.
الجزء 2 : باستخدام الحمض النووي الريبي تنظيف RNEasy Qiagen ميني كيت
وRNEasy Qiagen ميني كيت 2 هو مفيد في إزالة الملوثات والشوائب من عينة الحمض النووي الريبي معزولة عن طرق أخرى. لهذا الإجراء ، وهناك حاجة إلى β - المركابتويثانول ، والإيثانول ، والمياه الخالية من nuclease بالإضافة إلى المكونات المضمنة في المجموعة. ينصح علاج الدناز اختيارية خلال هذا الإجراء.
- عند أول استخدام لهذه المجموعة ، سوف الاحتياطي RPE ابد أن نكون مستعدين بإضافة 4 مجلدات من الإيثانول بنسبة 100 ٪ إلى 1 RPE حجم الاحتياطي.
- في يوم من هذا الإجراء ، والاحتياطي RLT ابد أن نكون مستعدين الطازجة. حساب المبلغ الإجمالي للRLT العازلة التي ستكون لازمة. وثمة حاجة إلى وحدة التخزين من 350 ميكرولتر لكل عينة. لإعداد RLT الاحتياطي ، إضافة 10 ميكرولتر من المركابتويثانول - β لكل 1 مل من العازلة. وينبغي أن يتم ذلك تحت غطاء الدخان.
- إلى كل عينة إضافة 350 ميكرولتر من RLT الاحتياطي و 250 ميكرولتر من الإيثانول بنسبة 100 ٪. مزيج جيد من قبل pipetting صعودا وهبوطا عدة مرات.
- نقل العينة ، التي ينبغي أن تكون حوالي 700 ميكرولتر ، إلى عمود RNEasy التي يتم وضعها في أنبوب جمع 2 مل وأجهزة الطرد المركزي في 8000 x ج لمدة 1 دقيقة في درجة حرارة الغرفة.
- بعد الطرد المركزي ، من خلال تجاهل تدفق وإضافة 700 ميكرولتر من الاحتياطي RW1 إلى عمود دوران RNEasy.
- العينة في جهاز الطرد المركزي 8000 x ج لمدة 1 دقيقة في درجة حرارة الغرفة ثم تتدفق من خلال تجاهل.
- الدناز المعاملة مع الدناز Qiagen كيت ريبونوكلياز خالية : الدناز العلاج هو اختياري ولكن يوصى بشدة لعينات من أعلى مستويات الجودة.
- عندما تتلقى أول طقم الدناز العلاج ، وسوف تحتاج إلى إعداد المخزون أنا الدناز الحل بإضافة 550 ميكروليتر nuclease خالية من الماء إلى الدناز. المزيج بلطف وقلب لا الدوامة. قسامة في قارورة تستخدم مرة واحدة تحتوي على 10 ميكرولتر من محلول المخزون. يمكنك تخزين الحل السهم عند -20 درجة مئوية لمدة تصل إلى 9 أشهر. ويمكن تخزين aliquots المذوبة في 4 درجات مئوية لمدة 6 أسابيع إذا لزم الأمر ، ولكن لا لاعادة تجميد aliquots بعد الذوبان.
- لتحضير مزيج حضانة أنا الدناز إضافة 70 ميكرولتر RDD الاحتياطي إلى 10 ميكرولتر ق أنا الدنازتوك حل لكل عينة. مزيج لطيف من خلال انقلاب وأنبوب الطرد المركزي لفترة وجيزة لجمع شكل سائل المتبقية على جانبي الأنبوب. إضافة 80 ميكرولتر حضانة أنا الدناز مزيج مباشرة إلى العمود تدور RNEasy. احتضان معاملة الدناز لمدة 30 دقيقة في درجة حرارة الغرفة.
- بعد إضافة 350 الدناز العلاج RW1 الاحتياطي ميكرولتر إلى العمود وتدور أجهزة الطرد المركزي في 8000 x ج لمدة 1 دقيقة في درجة حرارة الغرفة.
- بعد الطرد المركزي من خلال تجاهل تدفق وإضافة 500 RPE الاحتياطي ميكرولتر إلى العمود زيادة ونقصان. احتضان عينة لمدة 5 دقائق في درجة حرارة الغرفة.
- أجهزة الطرد المركزي في 8000 عينة XG لمدة 1 دقيقة في درجة حرارة الغرفة ، وتجاهل من خلال تدفق.
- بعد الطرد المركزي إضافة 500 ميكرولتر الايثانول 75 ٪ إلى عمود الدوران.
- كرر الطرد المركزي في 8000 XG ، ولكن لمدة 2 دقيقة في درجة حرارة الغرفة
- بعد الطرد المركزي من خلال تجاهل والسماح لتدفق العمود لتجف لمدة 5 دقائق.
- أجهزة الطرد المركزي على الفور في 8000 x ج لمدة 5 دقائق في درجة حرارة الغرفة لإزالة أي آثار متبقية من الايثانول.
- بعد الطرد المركزي هو نقل كامل العمود تدور في عالم جديد 1.5 مل أنبوب جمع وإضافة 10 ميكرولتر nuclease خالية من المياه. احتضان لمدة 1 دقيقة ثم الطرد المركزي في 10000 x ج لمدة 1 دقيقة في درجة حرارة الغرفة. وسوف يكون في الحمض النووي الريبي من خلال تدفق.
- إضافة آخر ميكرولتر 10 من nuclease خالية من المياه لعمود الدوران ويحضن في درجة حرارة الغرفة لمدة 1 دقيقة. أجهزة الطرد المركزي في 10000 عينة XG لمدة 1 دقيقة في درجة حرارة الغرفة.
- بعد الطرد المركزي لإزالة والتخلص من عمود الدوران. وسوف تكون في الحمض النووي الريبي من خلال التدفق.
- التحقق من كمية ونوعية من الحمض النووي الريبي باستخدام NanoDrop ND - 1000 معمل باتباع إرشادات الشركة المصنعة.
- بالإضافة إلى ذلك ، تشغيل هلام أو تغيير طبيعة استخدام اجيلنت bioanalyzer 2100 للتحقق من سلامة الحمض النووي الريبي.
- يجب أن يتم تخزين العينات في -80 درجة مئوية حتى يمكن تنفيذ التوليف [كدنا].
الجزء 3 : [كدنا] التجميعي باستخدام مرتفع Invitrogen لأول نظام ستراند
الحمض النووي الريبي هو عرضة للانقسام بسهولة بواسطة RNAses يؤدي إلى التدهور. ونتيجة لذلك تم تطوير العديد من بروتوكولات التعبير الجيني لاستخدام المنتج أكثر استقرارا [كدنا] التي تم تجميعها مباشرة من الحمض النووي الريبي. نحن هنا تجميع التفاصيل لأول حبلا [كدنا] باستخدام مرتفع Invitrogen النظام التجميعي لأول ستراند 3. يمكن لكل فعل التوليف [كدنا] تستوعب ما يصل إلى 5 ميكروغرام من الحمض النووي الريبي.
- قبل البدء في مزيج الداخلي وأجهزة الطرد المركزي لفترة وجيزة كل مكون.
- إعداد RNA / مزيج التمهيدي في العقيمة 0.5 مل أنبوب microfuge كما هو مبين في الجدول رقم 1.
- احتضان العينة على 65 درجة مئوية لمدة 5 دقائق.
- نقل على الفور إلى عينة الطين الثلج لمدة 10 دقيقة.
- بينما كانت العينة التبريد إعداد مزيج رئيسي مع المكونات المبينة في الجدول رقم 2. يتم سرد وحدات التخزين لكل 1 رد الفعل. ضبط كميات تبعا لعدد من ردود الفعل.
- بعد التبريد ، إضافة 9 ميكرولتر من مزيج الرئيسي أعد في الخطوة 5 لكل RNA / خليط التمهيدي. المزيج بلطف وجمع بواسطة الطرد المركزي وجيزة. وينبغي أن إجمالي حجم كل عينة إلى 19 ميكرولتر.
- احتضان عينة على 42 درجة مئوية لمدة 2 دقيقة في thermocycler.
- إضافة 1 ميكرولتر (50 وحدة) من مرتفع الثاني RT لكل أنبوب ، مزيج ، واحتضان حوالي 42 درجة مئوية لمدة 60 دقيقة في thermocycler.
- إنهاء رد الفعل عند 70 درجة مئوية لمدة 15 دقيقة ثم عينة البرد إلى 4 درجة مئوية. ويمكن برمجتها لthermocycler الخطوات 8 و 9.
- بعد العينة قد بلغ 4 درجات مئوية ، ونقل ردود الفعل على حمام جليدي.
- على الثلج إضافة 1 ميكرولتر من H ريبونوكلياز لكل أنبوب ، واحتضان لمدة 20 دقيقة عند 37 درجة مئوية. حجم إجمالية تبلغ الآن 21 ميكرولتر. وإضافة إلى H ريبونوكلياز عينتك تتحلل RNA القالب وتترك فقط للمنتج واحد طاق [كدنا].
الجزء 4 : [كدنا] العزل والأمطار
- وستستخدم 1.5 مل مرحلة قفل أنبوب هلام في عزلة من المنتج [كدنا]. تعد المرحلة 1.5 مل قفل أنبوب هلام بواسطة الطرد المركزي في 12000 x ج لمدة 2 دقيقة. ينبغي أن يكون كل الجل في الجزء السفلي من الأنبوب.
- إضافة 81.5 ميكرولتر الفينول (تريس المشبعة ، مخزنة على الرقم الهيدروجيني 8.0) ، 81.5 ميكرولتر من الكحول 24:1 isoamyl الكلوروفورم ، والعينة (21 ميكرولتر) في أنبوب هلام المرحلة القفل. مزيج عدة مرات من قبل انعكاس لطيف.
- العينة في جهاز الطرد المركزي 12000 XG لمدة 5 دقائق في درجة حرارة الغرفة.
- ينبغي أن يكون [كدنا] في المرحلة مائي العليا. نقل المرحلة العليا في تنظيف الأنبوب microfuge 1.5 مل. وينبغي أن يكون مجموع حجم حوالي 20 ميكرولتر.
- إضافة 1X حجم NaOAc م 3 ، ودرجة الحموضة 5.2 و المزيج بلطف. على سبيل المثال ، إذا كان حجم المرحلة العليا مائي يعادل 20 ميكرولتر ، وسوف تحتاج إلى إضافة 2 ميكرولتر من NaOAc م 3 ، ودرجة الحموضة 5.2.
- إضافة 7 ميكرولتر من الجليكوجين ملغ / 5 مل ومزيج بلطف.
- إضافة 1X حجم الأيزوبروبانول ومزيج بلطف. عموما هذه هي حوالي 30 ميكرولتر من الأيزوبروبانول.
- السماح لاحتضان عينة temperatur في الغرفةه لمدة 10 دقيقة ثم الطرد المركزي في 12000 x ج لمدة 20 دقيقة في درجة حرارة الغرفة.
- وينبغي أن يكون شكل الكريات الصغيرة [كدنا] على الجزء السفلي من الأنبوب. إزالة بعناية طاف مع ماصة.
- إضافة 500 ميكرولتر من الإيثانول بنسبة 70 ٪ وخليط من خلال انقلاب.
- العينة في جهاز الطرد المركزي 12000 XG لمدة 5 دقائق.
- بعد الطرد المركزي إزالة طاف مع ماصة وتكرار غسل الإيثانول 70 ٪ والطرد المركزي (الخطوات 10 و 11).
- بعد الطرد المركزي إزالة طاف مع ماصة. إذا كان هناك السائل المتبقي على جانبي القناة ، ويمكن جمعها من خلال الدوران لفترة وجيزة في الأنبوب. إزالة أي السائل الزائد والسماح بيليه لتجف في درجة حرارة الغرفة لمدة 5 دقائق.
- إضافة ميكرولتر من 20 nuclease خالية من المياه لترطيب وبيليه. مكان العينة على 55 درجة مئوية لمدة 5 دقائق لمعالجة الجفاف من بيليه.
- ثم يتم التحقق من كمية ونوعية المنتج [كدنا] باستخدام NanoDrop ND - 1000 معمل باتباع إرشادات الشركة المصنعة. ويمكن تخزين [كدنا] في -20 درجة مئوية.
ممثل النتائج
بعد تنظيف الحمض النووي الريبي ، يمكن توقع ما يقرب من 15 ميكروغرام من الحمض النووي الريبي عالية الجودة الشاملة من الأجنة الزرد 50. ويمكن لتقييم جودة مجموع الحمض النووي الريبي ، معمل أ ، هلام إستشراد ، و2100 Bioanalyzer اجيلنت استخدامها. ويمكن استخدام ND - 1000 NanoDrop معمل لتقييم الامتصاصية في 260 نانومتر مقارنة الامتصاصية عند 280 نانومتر (الشكل 1). ويمكن لل260 / 280 ألف نسبة تكشف عن وجود ملوثات وتعطي دليلا على تدهور محتمل. وهناك 260 / يعتبر نسبة 280 من 1،9-2،0 مقبولة. بالإضافة إلى ذلك ، يوصى بشدة أن يكون تشغيل هلام تمسخ الرنا RNA لتقييم سلامة. وجدائل الحمض النووي الريبي منفصلة على أساس حجمها ، مع أصغر فروع يهاجرون إلى مزيد من الانخفاض في هلام. وهناك عينة غير المتدهورة تظهر مسحة مع اثنين من الفرق القوية. مسحة هو نتيجة لمجموعة من السكان من مختلف فروع مرنا الحجم وتتوافق مع العصابات والرنا الريباسي 28S 18S. وينبغي أن تكون الفرقة 28S حوالي مرتين بنفس حدة الفرقة 18S (الشكل 2). بدلا من ذلك ، يمكن تقييم سلامة الحمض النووي الريبي مجموع باستخدام اجيلنت bioanalyzer 2100. ومن المتوقع ان اثنين من القمم متميزة تمثل والرنا الريباسي 28S 18S (الشكل 3). ينبغي أن تكون ذروة 28S 18S أكبر من الذروة مع المنطقة تحت قمم حوالي 2:1 ، على التوالي. ولن تكون متميزة بين قمتين لوحظت في عينات المتدهورة. لا ينبغي أن عينات الحمض النووي الريبي العارضة تدهور تتم من خلال إجراءات تجريبية لاحقة.
ويمكن استخدام التحليل الطيفي لتقييم جودة المنتج [كدنا] (الشكل 4). وينبغي على 260 / 280 ألف إلى حوالي 1.8. ردود الفعل [كدنا] مع مدخلا من 5 ميكروغرام من الحمض النووي الريبي مجموع العائد بشكل روتيني 1-2 ميكروغرام من الناتج [كدنا] في المختبر لدينا.

الشكل 1. طيف NanoDrop عينة الحمض النووي الريبي ، وبعد تنظيف الحمض النووي الريبي ، يمكن تقييم كمية ونوعية الحمض النووي الريبي باستخدام ND - 1000 NanoDrop معمل. وأثمرت بشكل روتيني حوالي 15 ميكروغرام من الحمض النووي الريبي جودة عالية من مجموع 50 الأجنة الزرد مع A 260 / 280 وحول نسبة 1،9-2،0.
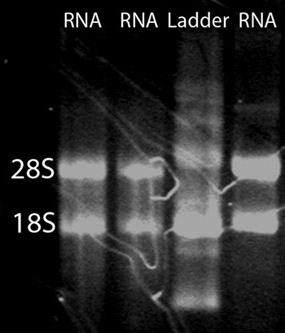
الشكل 2. ثمة هلام تمسخ الحمض النووي الريبي. لتقييم سلامة وعزل الحمض النووي الريبي مجموع ، يمكن أن يكون جل تمسخ RNA ركض. ومن المتوقع أن مسحة مع اثنين من الفرق المقابلة للمشرق والرنا الريباسي 28S 18S. ينبغي أن تكون الفرقة 28S تقريبا ضعف شديد كما الفرقة 18S.
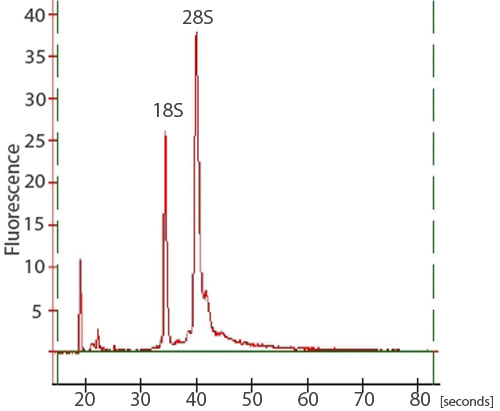
الشكل 3. تتبع عينة من الحمض النووي الريبي من bioanalyzer. لتقييم سلامة وعزل الحمض النووي الريبي مجموع يجوز أيضا عينات يتم تحليلها على bioanalyzer اجيلنت 2100. وينبغي أن اثنين من قمم حادة ، المقابلة ل28S 18S الرنا الريباسي و، تكون مرئية. ينبغي أن تكون ذروة 28S 18S أكبر من الذروة مع المنطقة تحت قمم حوالي 2:1 ، على التوالي.
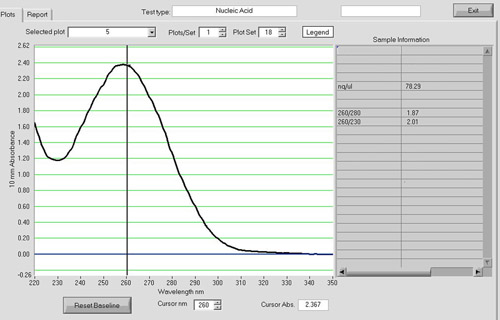
الشكل 4. ويمكن استخدام الطيف NanoDrop عينة [كدنا]. تحليل الطيف مع 1000 - ND NanoDrop لتقييم كمية ونوعية المنتج [كدنا]. وينبغي لل260 / 280 ألف نسبة بحوالي 1.8. ردود الفعل [كدنا] مع مدخلا من 5 ميكروغرام من الحمض النووي الريبي مجموع العائد بشكل روتيني 1-2 ميكروغرام من [كدنا] في المختبر لدينا.
الجدول 1. مكونات الحمض النووي الريبي لإضافة ل/ مخاليط التمهيدي في الخطوة 2 من التوليف [كدنا].
| مكون | حجم |
| مجموع الحمض النووي الريبي (حتى 5 ميكروغرام) | 10 ميكرولتر |
| 10 ملي مزيج dNTP | 1 ميكرولتر |
| أليغو (DT) 12-18 (0.5 ميكروغرام / ميكرولتر) | 1 ميكرولتر |
| DEPC المياه المعالجة | ن ميكرولتر |
| اجمالى حجم | 10 ميكرولتر |
خليط التفاعل الجدول 2. الخطوة 5 من أجل تخليق [كدنا]. أحجام المذكورة هي في رد الفعل. زيادة حجم كل مكون لمجموع عدد من ردود الفعل.
| مكون | حجم |
| 10X RT العازلة | 2 ميكرولتر |
| 25 ملم MgCl2 | 4 ميكرولتر |
| 0.1 ملم DTT | 2 ميكرولتر |
| RNAseOUT | 1 ميكرولتر |
Discussion
هشاشة جزيء الحمض النووي الريبي هو الاعتبار الأهم الذي ينبغي ألا يغيب عن البال طوال هذا البروتوكول. وينبغي دائما أن المعدات المعقمة ريبونوكلياز خالية تستخدم في منطقة خالية من ريبونوكلياز المختبر. ومن المفيد أن تحتفظ بجزء من المختبر لاستخدامها في إجراءات RNA فقط. يجب رش هذا المجال في كثير من الأحيان مع منتج ريبونوكلياز إزالة مثل ريبونوكلياز بعيدا. وينبغي دائما على عينات الحمض النووي الريبي يتم التعامل معها قفازات وأبقى على الجليد لمنع تدهورها.
استغرق هذا البروتوكول الاستفادة من الكواشف المتاحة تجاريا ومجموعات. بدلا من ذلك ، هناك العديد من الكواشف إضافية ومستلزمات العزل RNA المتاحة في السوق لمجموع العزلة RNA. عملت كواشف ومستلزمات المدرجة في هذا البروتوكول بشكل جيد وحققت بشكل روتيني RNA عالية الجودة في مختبر لدينا.
كبديل ، يمكن أن يؤديها مزدوجة التوليف [كدنا] الذين تقطعت بهم السبل ، وبدلا من تجميع الشكل الأول أظهر في هذا البروتوكول. هو المطلوب في بعض الأحيان المزدوج [كدنا] الذين تقطعت بهم السبل ، حيث أنه يوفر الاستقرار المتزايد. بالإضافة إلى ذلك ، تتطلب بعض المنتجات [كدنا] بروتوكولات الذين تقطعت بهم السبل المزدوج كمدخل. ومع ذلك ، إذا كانت العينات ستكون أبقى في المنزل لتطبيقات المصب ، أولا توليف حبلا غير كافية وأكثر اقتصادا.
Disclosures
The authors have nothing to disclose.
Materials
| Name | Company | Catalog Number | Comments |
| Glycogen (5 mg/ml) | Ambion | 9510 | |
| NanoDrop ND-100 | Thermo Fisher Scientific, Inc. | ND-1000 | |
| Pellet Pestles with Microfuge Tube | VWR international | KT749520-0090 | |
| Phase Lock Gel Light, 1.5 ml | Eppendorf | 2302800 | |
| Phenol, Tris-saturated | Roche Group | 3117944001 | |
| RNAse Away | VWR international | 17810-491 | |
| RNAse-Free DNase Set | Qiagen | 79254 | |
| RNEasy Mini Kit | Qiagen | 74104 | |
| SuperScript® First-Strand Synthesis System for RT-PCR | Invitrogen | 11904-018 | |
| TRIzol | Invitrogen | 15596-026 |
References
- TRIzol Reagent Manual. , (2007).
- RNEasy Mini Handbook. , 4th ed, (2006).
- SuperScript First-Strand Synthesis System for RT-PCR. , Version E. (2003).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved